水生生物に安全なpHとされているのは、6.8〜8.5であり、この範囲を超えると栄養塩は植物に摂取されにくくなり、餌料生物の生産性は低下し、ひいては水域全体の生産も低下するとされている。
| 酸性(pH2) | 横転〜鰓から出血〜死亡(30分後) |
| アルカリ性(pH12) | 体表から粘液〜横転〜鰓から出血〜死亡(2時間後) |
湖沼水は、特に夏季の成層期には、表層は植物プランクトンの光合成によって二酸化炭素が消費されるためにアルカリ側に傾き、底層はプランクトンの遺骸の分解に伴って二酸化炭素や有機酸が生成するため酸性側に傾く。河川でも、水深が浅く(日光が河床まで届く)水が停滞するような場所では、河床の付着藻類の光合成のためにpH値が高くなり、同時に溶存酸素も高くなることがある。
光合成は藻類が葉緑素と日光のエネルギーのもとに、水中の二酸化炭素(CO2)と水を使ってデンプンと酸素(O2)に変える作用である。水中のCO2は少量であるため、藻類は、炭酸水素イオン(HCO3-)をカルボニックアントヒドラ−ゼの触媒作用によってH2CO3とし、脱水反応でCO2として利用する。その結果、停滞水域であれば、水中のHCO3-は減少し、O2が増加し続けることになる。
水中の炭酸ガスは次式の化学平衡にあり、水質のpH値を左右する。
CO2+H2O⇔H2CO3⇔HCO3+H+⇔CO32-+2H+
光合成によってHCO3-が減少すれば昼間のpH値は上昇することになる。しかし、夜間は藻類の呼吸作用により、逆に水中のO2を消費してCO2を放出し、HCO3-濃度が高くなるためpH値は低くなり、溶存酸素(DO)も減少することになる。
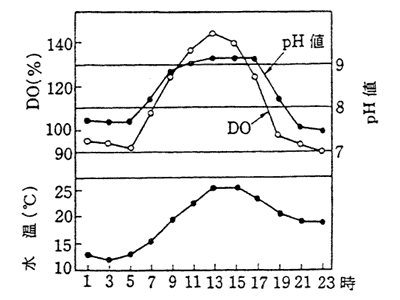 出典:合山幹二、水環境指標(1979)
出典:合山幹二、水環境指標(1979)